陕西乾县第一中学 ( 713300)
实验是化学的精髓,是化学学科调动学生兴趣的最好手段。高一高二的新授课,凡是有实验的化学课,学生兴趣盎然,课堂气氛活跃,师生、生生互动良好。到了高三,老师们就不再做实验了。复习课的模式基本相同:罗列知识点——分析重难点——强调易错点——举例练习巩固。学生兴趣不高,参与度低,课堂气氛压抑,复习效果不佳。
高三复习课就不用做实验了吗?如果高三复习课上做实验,能否起到调动学生的复习热情,提高复习课效果的作用呢?基于以上思考及我校提出的梳理-探究-训练的高校课堂教学模式,我设计“电解池”一节复习课的教学过程如下,请同行指正。
趣味实验演示,燃起学生的复习兴趣
“成功的教学需要的不是强制,而是激发学生的兴趣”。这句话不仅适用于新课程下的新授课,更适用于高三的复习课,可以说,高效的复习需要的不是强制,而是激发学生的复习兴趣和积极性。兴趣能产生激情,在兴趣的催化下,学生能树立起信心,朝气蓬勃、积极向上的学习,能更愉快的参与到复习中来[1]。
趣味实验演示:在一块罐头盒铁皮上贴一张浸透了饱和NaCl溶液的滤纸,并与电池的负极相连;在电池的正极连接一个碳棒作“笔”。在滤纸上滴加淀粉-KI溶液,便能写出蓝色的字。
自主梳理知识,调动学生的复习积极性
学生带着好奇心看完实验现象后,心情激动,有解释实验现象的欲望(已有的电解知识储备完全可以解释实验现象),我便趁机提出问题:
[多媒体展示]
①电解池两极分别生成何种产物?
②为什么能写出蓝色的字?说明什么问题?
③你判断产物的依据是什么?
学生1:电解池阳极产生氯气,阴极产生氢气。
学生2:蓝色的字是因为淀粉溶液变蓝了,说明阳极生成的氯气将碘离子氧化成了碘单质,淀粉溶液遇碘单质变蓝。
学生3:阴阳离子的放电顺序。
教师:回答的很好。现在请大家回顾旧知,试着写出:一般情况下,阴阳两极阳、阴离子的放电顺序。
(学生跃跃欲试,尝试着完成老师布置的小任务。叫一名学生写到黑板的主板位置)
(教师巡视、指导、纠错,待写完后先肯定学生写得好的方面,纠错并补充学生忽视的问题:判断两极产物时,要特别注意阳极材料,阳极为银及其之前的金属活性电极时,电极材料放电,并将“活性电极”四个字用红色粉笔加到学生写的阴离子的放电顺序之前,帮助学生完成知识的梳理。)
问题过渡:
[多媒体展示]
1.你能否写出上述电解实验的两极及总反应式?
2.你能写出用惰性电极电解H2SO4(aq)、MgCl2(aq)的总反应方程式吗?
此时学生的兴趣浓厚,加之电解饱和食盐水的电极反应式在训练离子方程式的书写时已写过,学生并不觉得难写,因而积极性很高,有练习的冲动。
(学生活动:动笔练习。再叫两名学生上黑板书写)
根据以上练习,由学生分组讨论得出分析电解反应的一般思路及电极反应式书写时的注意事项。教师引导、点拨并将结果用多媒体展示。
[多媒体展示]
1.分析电解反应的一般思路:
明确电极材料和溶液中存在哪些离子
分析阴阳两极附近有哪些离子
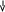
根据阳极氧化、阴极还原分析得出产物
2.电解时离子的放电顺序:
阳离子放电顺序:Ag+> Hg2+ > Fe3+ >Cu2+>H+>Pb2+ >Fe2+>Zn2+>Al3+>Mg2+>Na+ >Ca2+>K+
阴离子放电顺序:活性电极>S2->I->Br->Cl- >OH->含氧酸根离子
3
阴极——(与外接电源负极相连),发生还原反应
 .
.
阳极——(与外接电源正极相连),发生氧化反应
电极反应
4.电解方程式的书写(注意事项):
①必须标明“电解”二字;
②阳极反应式书写前,先看电极再看阴离子;
③书写电解总反应式时,弱电解质要写成分子式;
④确保电子转移数目、原子个数守恒。
课堂活动进行到这儿,学生并不满足(就像吃得半饱的孩子,渴望更多的好东西),因此我趁热打铁,让学生继续交流讨论用惰性电极电解电解质溶液的规律。
[多媒体展示]
用惰性电极电解电解质溶液的类型:
实例 | 阴极反应式 | 阳极反应式 | 总反应式 | 实际电解物质 | 溶液pH 变化 | 电解质溶液复原方法 |
强碱(NaOH) | | | | | | |
含氧酸(H2SO4) | | | | |||
活泼金属含氧酸盐(Na2SO4) | | | | |||
无氧酸(HCl) | | | | | | |
不活泼金属无氧酸盐(CuCl2) | | | | | | |
活泼金属的无氧酸盐(NaCl、MgCl2) | | | | | | |
| | | ||||
不活泼金属含氧酸盐(CuSO4、AgNO3) | | | | | | |
| | |
学生活动:分组讨论、交流,完成表格内容后展示成果。
[多媒体展示]
思考:
电解完NaCl溶液后,要恢复原浓度,能否加入盐酸?(否)
电解完CuSO4溶液后,要恢复原浓度,能否加入Cu(OH)2?(否)
(学生作答,老师指正。)
总结:恢复电解质溶液,应遵循“缺什么加什么,缺多少加多少”的原则。一般加入阳极产物与阴极产物的化合物。加入物质的物质的量需根据电路中的电子守恒进行计算。
典例训练巩固,提高学生对知识的迁移能力
[多媒体展示]
1 . 某学生欲完成 2HCl + 2Ag = 2AgCl+H2↑反应,设计了下列四个实验,你认为可行的实验是( )
. 某学生欲完成 2HCl + 2Ag = 2AgCl+H2↑反应,设计了下列四个实验,你认为可行的实验是( )
2. 用指定材料做电极来电解一定浓度的溶液甲,然后加入物质乙能使溶液恢复为甲溶液原来的浓度,则合适的组是( )
| 阳极 | 阴极 | 溶液甲 | 物质乙 |
A. | Pt | Pt | NaOH | NaOH固体 |
B. | Pt | Pt | H2SO4 | H2O |
C. | C | Fe | NaCl | 盐酸 |
D. | Cu | C | CuSO4 | Cu(OH) 2 |
(以上两题同桌间讨论完成,并由学生自己评价题目)
生1:第1题考查电解原理:根据电解总反应判断电极材料、电解质溶液。
生2:第2题考查电解规律,电解质溶液的复原。
高考真题体验,提升学生的学科素养
[多媒体展示]
3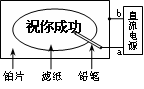 .某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是( )
.某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是( )
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
4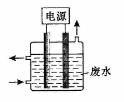 .用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,
.用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,
下列说法不正确的是( )
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl-+ 2OH--2e-= ClO- + H2O
C.阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + ![]() 5Cl-+ H2O
5Cl-+ H2O
[参考答案]1.C,2.B,3.D,4.D
[反思]:高效的复习课不仅需要教师精心准备,更需要学生的高度参与与配合。传统的复习课基本上是教师唱独角戏,学生被动接受知识,课堂参与度不高。为使复习课教学有所改观,本节课我以“四步曲”组织、设计教学内容,对课前趣味实验现象的分析燃起了学生的复习兴趣,使学生能够全身心的投入到复习中来,复习积极性高,课堂参与度高涨;同时,以实验为核心,实现了对“电解池”一节知识点的串联和并联,帮助学生解决知识的梳理和构建,引导学生在教学互动中积极思考,巩固所学知识(尤其是重难点),真题实战练习提高了学生提取和运用知识的能力,提高了教学实效。
参考文献:
[1]黄浣波.谈创新实验在中学化学教学中的应用[J].中学化学教学参考,2015(7):38.