空军军医大学第一附属医院( 陕西 西安) 710032
摘要:目的 使用多个浓度患者样本评估临床生化常规检验项目的测量不确定度,探讨不同的测量不确定如何使用。方法 分别收集碱性磷酸酶(ALP)、谷氨酰转肽酶(GGT)、丙氨酸转氨酶(ALT)和天门冬氨酸转氨酶(AST)检测项目的样本。每个检测项目5个浓度,每个浓度10个样本,共50个样本双份测定。按照多个浓度患者样本评估测量不确定度的方式评估A类不确定度,使用校准品引入的分量作为B类不确定度,最终评估相对不确定度和绝对不确定度在临床使用中的异同。结果 ALP项目5个浓度的绝对不确定度分别是16.04、23.01、32.07、38.84、41.81, 相对不确定度分别是20.13、15.77、18.37、13.78和9.27,在浓度67 IU/L处有相交。GGT项目5个浓度的绝对不确定度分别是13.58、25.79、17.45、21.08和23.75, 相对不确定度分别是58.38、45.66、20.67、16.68和15.83,在浓度105 IU/L处有相交。ALT项目5个浓度的绝对不确定度分别是15.10、16.97、29.12、42.29和67.44, 相对不确定度分别是25.61、20.93、24.67、21.86和14.45,在浓度108 IU/L处有相交。AST项目5个浓度的绝对不确定度分别是15.88、17.09、24.74、44.41和58.41, 相对不确定度分别是26.45、20.41、19.19、21.26和17.08,在浓度106 IU/L处有相交。差异有统计学意义(P<0.05)。
结论 使用多个浓度患者样本评估测量不确定度,有助于最大程度的减少误差,给出合理的测量不确定度应用范围。
关键词:生化;不确定度;评估;浓度
ISO15189:2012中明确要求,在临床检验过程中,用于报告测量患者样品的被测量值的测量程序应评估不确定度。测量不确定度的评估提高了结果的质量和可靠性[1]。目前不确定度一般采用自上而下法(Top-Down法)或自下而上法(bottom-up法)。Top-Down法是基于室内质控(IQC)数据和室间质评(EQA)结果同时使用统计学原理检测不确定度[2]。Bottom-Up法是基于对测量不确定度来源进行综合分析,分别评定各不确定度分量,然后进行合成。本文在此基础上使用多个浓度患者样本对生化检验项目进行测量不确定度评定,为供临床实验室在结果解释过程中提供参考依据。
1 材料与方法
1.1 材料采用全自动生化分析仪(日本日立,型号7180)试剂及配套校准品(日本和光、四川迈克提供)、室内质控品与定值质控品(朗道提供)。选取相关浓度的血清样本共50例。
1.2 方法检测开始前先确定仪器性能良好,将其正常校准。对本次选取的50例患者进行生化检测,抽取空腹患者5ml的静脉血液,采取离心操作并分离血清,以速率法测定患者碱性磷酸酶(ALP)、谷氨酰转肽酶(GGT)、丙氨酸转氨酶(ALT)及天门冬氨酸转氨酶(AST)水平;其中每个指标分为5个浓度梯度,每个梯度检测10个患者标本并重复2次。
1.3 观察指标分析各生化指标检测结果的不确定度不确定度来源于测量样品的精密度和测量样品的不确定度。测量的精密度仅分析统计学处理中估计值的不确定度,是校准品来源的不确定度分量的平方与精密度来源的平方之和的平方根;测量样品的不确定度是合成标准不确定度与包含因子数的乘积。
1.4 统计学分析对本文所得数据均采用SPSS统计学软件进行检验,计量资料采用t检验,计数资料采用X2检验,P<0.05有统计学意义。
2 结果
分别计算出以下四种不确定度
2![]()
.1 A类不确定度:Sp和RSDp
其![]()
![]()
中Δi为样本两次测量结果的偏移;
Δirel为样本两次测量结果的相对偏移。
2![]()
.2 B类不确定度:uc(bias)和ucrel(bias)其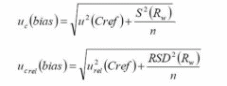
中uc(bias)为校准品偏移引入的测量不确定度,ucrel(bias)校准品偏移引入的相对测量不确定度
2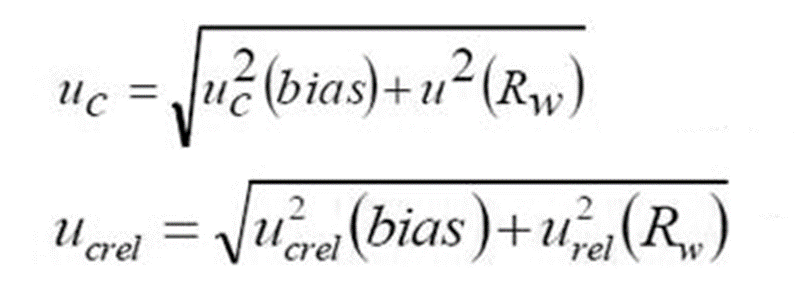
.3合成相对标准不确定度根据不确定度传播率,合成相对标准不确定度的计算方法:
2.4相对扩展标准不确定度的计算方法:u=2×uc, uCrel= 2×ucrel
2.5 ALP, GGT, ALT, AST 的四项不确定度见表1;
表1 ALP,GGT,ALT,AST不确定度
项目 | 浓度 (IU/L) | A类 | B类(合成) | 合成不确定度 | 扩展合成不确定度 | ||||
Sp | RSDp | uC(bias) | ucrel(bias) | uC | ucrel | U | Urel | ||
ALP | 50 | 5.00 | 9.87 | 6.50 | 1.98 | 8.20 | 10.07 | 16.40 | 20.13 |
120 | 9.49 | 7.63 | 6.50 | 1.98 | 11.50 | 7.88 | 23.01 | 15.77 | |
150 | 14.66 | 8.97 | 6.50 | 1.98 | 16.04 | 9.19 | 32.07 | 18.37 | |
260 | 18.30 | 6.60 | 6.50 | 1.98 | 19.42 | 6.89 | 38.84 | 13.78 | |
350 | 19.87 | 4.19 | 6.50 | 1.98 | 20.91 | 4.63 | 41.81 | 9.27 | |
GGT | 20 | 6.71 | 29.18 | 1.05 | 0.73 | 6.79 | 29.19 | 13.58 | 58.38 |
50 | 12.85 | 22.82 | 1.05 | 0.73 | 12.89 | 22.83 | 25.79 | 45.66 | |
80 | 8.66 | 10.31 | 1.05 | 0.73 | 8.72 | 10.34 | 17.45 | 20.67 | |
120 | 10.49 | 8.31 | 1.05 | 0.73 | 10.54 | 8.34 | 21.08 | 16.68 | |
150 | 11.83 | 7.88 | 1.05 | 0.73 | 11.88 | 7.91 | 23.75 | 15.83 | |
ALT | 50 | 7.42 | 12.77 | 1.40 | 0.95 | 7.55 | 12.81 | 15.10 | 25.61 |
80 | 8.37 | 10.42 | 1.40 | 0.95 | 8.49 | 10.46 | 16.97 | 20.93 | |
120 | 14.49 | 12.30 | 1.40 | 0.95 | 14.56 | 12.34 | 29.11 | 24.67 | |
200 | 21.10 | 10.89 | 1.40 | 0.95 | 21.15 | 10.93 | 42.29 | 21.86 | |
300 | 33.69 | 7.16 | 1.40 | 0.95 | 33.72 | 7.22 | 67.44 | 14.45 | |
AST | 50 | 7.75 | 13.17 | 1.73 | 1.22 | 7.94 | 13.23 | 15.88 | 26.45 |
80 | 8.37 | 10.13 | 1.73 | 1.22 | 8.55 | 10.20 | 17.09 | 20.41 | |
120 | 12.25 | 9.51 | 1.73 | 1.22 | 12.37 | 9.59 | 24.74 | 19.19 | |
200 | 22.14 | 10.56 | 1.73 | 1.22 | 22.21 | 10.63 | 44.41 | 21.26 | |
300 | 29.15 | 8.45 | 1.73 | 1.22 | 29.21 | 8.54 | 58.41 | 17.08 | |
2.6以待检样本的浓度为横坐标,合成不确定度为纵坐标如图所示,每幅图都出现一个交点,此交叉点即为绝对不确定度和相对不确定度的拐点。ALP,GGT,ALT,AST的拐点位置分别为67,105,108,106。

3讨论
随着生化检验技术的不断成熟,患者标本各项指标赋值的准确性对于疾病的诊断和疗效的判定有着重要的意义。目前评估患者标本赋值的准确性有不确定度和总误差分析。它们之间唯一的区别是在相同的数据上利用不同的数学概念来计算。在临床决策中,使用测量不确定度解释实验室结果能更好的监测医疗诊断和治疗效果[3-4]。
测量不确定度是探讨某一测量方法的总变异,是测量过程中每一影响因素的合成,为临床说明检测结果的可信区间即表征合理赋予被测量的值的分散性[5-6]。国内外关于医学实验室是否有必要引入测量不确定度的争论仍较多,无论是评定测量前过程的不确定度或总误差都很复杂[7-8]。自上而下法有着计算缺乏标准化和没有提供如何处理偏差指导的局限性。目前,国内外评定常规项目不确定方法基本上大多是将偏移的不确定度和从精密度导出的不确定度作为合成不确定度的主要来源[9-12]。李晶[13]采用“自上而下”和“自下而上”两种方法 评定同一检测系统测定六项肿瘤标志物的测量不确定度。文中认为,由于检测项目的不确定度主要来源于检测系统和环境的波动,人为因素难以减小不确定度。“自下而上”法利用现有的数据评定不确定度更加省时省力。
本文是引入两种不确定度分量:A类不确定度和B类不确定度,之后将合成不确定度与扩展合成不确定作为判断拐点的主要来源。A类不确定度是通过观测列数据求得标准偏差,继而算出标准不确定度;B类评定则是先估计被评定的(变)量的变化范围(±a),再按变量可能的分布情况反算标准偏差(即标准不确定度)。研究发现随着浓度的升高,Sp逐渐升高而RSDp逐渐下降,如果用单一的不确定来评价标准化工作具有一定的局限性。本文结合两种不确定度评估方法,小于这个浓度使用绝对不确定度,大于这个浓度用相对不确定度。使得实验室提供的数据更适应不确定度的规则限制,以获得符合临床结果的测试方法,建立完善的质量体系,同时也为此后实验室原始数据的评定提供了一定的依据。
参考文献:
曾晓君,李景碧.参考测量程序测定血清三酰甘油水平的测量不确定度评[J].检验医学与临床, 2019,16(08):1044-1046
Çubukçu HC, Yavuz Ö, Devrim E. Uncertainty of measurement for 14 immunoassay analytes: application to laboratory result interpretation [J]. Scand J Clin Lab Invest. 2019 Feb-Apr;79(1-2):117-122.
Balık AR, Gücel F. Evaluation of 20 clinical chemistry and 12 immunoassay analytes in terms of total analytical error and measurement uncertainty [J]. Scand J Clin Lab Invest. 2021 Nov;81(7):517-522
王玉兰,杨慧丽,王晓慧,等.自上而下法评定生化测量不确定度在国际旅行卫生保健中心实验室中的应用[J].中国卫生检验杂志,2017,27(20):1044-1046.
冯仁丰. 临床实验室分析质量目标的共识(上) [J]. 检验医学. 2016, 31 (2): 1-8.
White G H. Metrological traceability in clinical biochemist[J].Ann Clin Bio chem, 2011, 48(5):398-409.
Westgard JO. Useful measures and models for analytical quality management in medical laboratories[J]. Clin Chem Lab Med, 2016, 54(2): 223–233.
徐润灏,张 洁.8项生化指标测量不确定度评估及允许范围的初步研究[J].上海交通大学学报,2016,12(20):7
李峥嵘, 唐继海, 朱林涛等.测定不确定度在临床生化检验中的应用[J].检验医学与临床, 2012, 9(17):2126-2127.
梁结玲, 袁耀钦, 陈健发等.生化项目不确定度不同评定方法的临床应用评价[J]. 中国医药导报,2013,13(10):90-92.
肖雪野.探讨测量不确定度在临床常规生化检验中的应用[J]. 世界最新医学信息文摘,2018,26(32): 150-151.
尹晶平, 董菁, 徐杰等.测量不确定度评估临床干生化检验的初步应用[J]. 检验医学与临床,2015,20(12):2033-2037.
李晶,张绍军,黄延荣等.采用“自上而下”和“自下而上”两种方法评定同一检测系统测定六项肿瘤标志物的测量不确定度[J]. 中国医药导报, 2020,17(01):169-173